Du kan ændre denne formel, hvis du vil finde ændringen i mængden af varme i stedet for den specifikke varme. Ligningen bliver så: ΔQ = mCsT 

m = 350 g Q = 34.700 Joule ΔT = 173ºC - 22ºC = 151ºC Cs = ukendt 
Den oprindelige ligning: Cs = Q/mΔT c = 34.700 J/(350 g x 151ºC) 
Cs =34.700 J/(350 g x 151ºC) Cs =34.700 J/(52850g x ºC) Cs = 0,65657521286 J/(g x ºC)
Beregn specifik varme
Specifik varme er den mængde energi, der kræves for at hæve temperaturen på 1 gram af et stof med 1 grad Celsius. Et stofs specifikke varme afhænger både af molekylstrukturen og den fase, stoffet er i. Opdagelsen af specifik varme satte skub i studiet af termodynamik, studiet af energiomdannelse ved varme og driften af systemer. Specifik varme og termodynamik bruges i vid udstrækning inden for kemi, nuklear forskning og aerodynamik, såvel som i hverdagen i det centrale varme- og kølesystem i din bil. Hvis du vil vide, hvordan man beregner specifik varme, skal du tage følgende trin.
Trin
Metode 1 af 2: At lære det grundlæggende

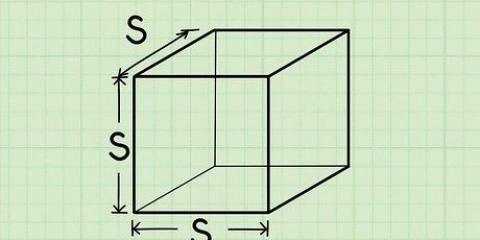
1. Gør dig bekendt med de termer, der bruges til at beregne specifik varme, før du lærer om formlerne, der skal bruges. Lær at genkende de forskellige udtryk og hvad de betyder. Her er de termer, der oftest bruges ved beregning af et stofs specifikke varme: Massen er repræsenteret ved "m". Mængden af varme er repræsenteret ved "Q". Mængden af varme er repræsenteret ved "J", eller Joules. "t" er stoffets temperatur. Specifik varme er repræsenteret ved "Cs".
- Delta, eller det "Δ" symbol, repræsenterer ændringen af en variabel.
- For eksempel, hvis den første temperatur (T1) er 150ºC og den anden (T2) 20ºC, så er ΔT eller ændringen i temperaturen lig med 150ºC - 20ºC eller 130ºC.

2. Ligningen for specifik varme. Når du er bekendt med de termer, der bruges til at beregne specifik varme, bør du nu lære deres ligning. Formlen er: Cs = Q/mΔT.
Metode 2 af 2: Beregning af specifik varme

1. Et nærmere kig på sammenligningen. Hvad er nødvendigt for at beregne specifik varme. Antag at du har følgende problem: Beregn den specifikke varme på 350 g af et ukendt stof, hvis du har 34.Tilsæt 700 Joule varme, og temperaturen stiger fra 22ºC til 173ºC uden faseskift.

2. Liste kendte og ukendte faktorer. Når problemets nyhed forsvinder, kan du begynde at skrive hver kendt og ukendt variabel ned for at få en bedre ide om, hvad du har med at gøre med. Her er hvad du skal gøre:

3. Sæt de kendte faktorer ind i ligningen. Du kender værdien af alt andet end "Csc", så du bliver nødt til at bruge resten af faktorerne i ligningen og løse for "Cs". Sådan fungerer det:

4. Løs ligningen. Nu hvor du har brugt alle de kendte faktorer i ligningen, er resten let matematik. Den specifikke varme er 0,65657521286 J/(g x ºC).
Tips
- SI (Systeme International) definerer specifik varme som Joule per grad Celsius per gram. Men antallet af kalorier pr. grad Fahrenheit pr. pund bruges stadig i det kejserlige enhedssystem.
- Metal opvarmes hurtigere end vand, fordi det har en lav specifik varme.
- Et kalorimeter kan nogle gange bruges under en kemisk reaktion, når varme transporteres.
- Ved løsning af sådanne problemer er det vigtigt at annullere enhederne mod hinanden, hvor det er muligt.
- Den specifikke varme af mange genstande kan findes i specielle opslagsbøger eller online.
- Temperaturændringen er større i materialer med lav specifik varme, forudsat at alle andre forhold forbliver uændrede.
- Formlen til beregning af madens specifikke varme. Cs = 4.180 x b + 1.711 x p + 1.928×f+1.547 x c + 0.908 x a er ligningen, der bruges til at beregne den specifikke varme af mad. "W" er procentdelen af vand, "s" er procentdelen af protein, "f" er fedtprocenten, "c" er procentdelen af kulhydrater og "-en" er procentdelen af kulstof. Denne ligning tager højde for massen (x) af alle de faste stoffer, der udgør maden. Den specifikke varme er udtrykt i kJ/(kg-K).
Artikler om emnet "Beregn specifik varme"
Оцените, пожалуйста статью
Populær